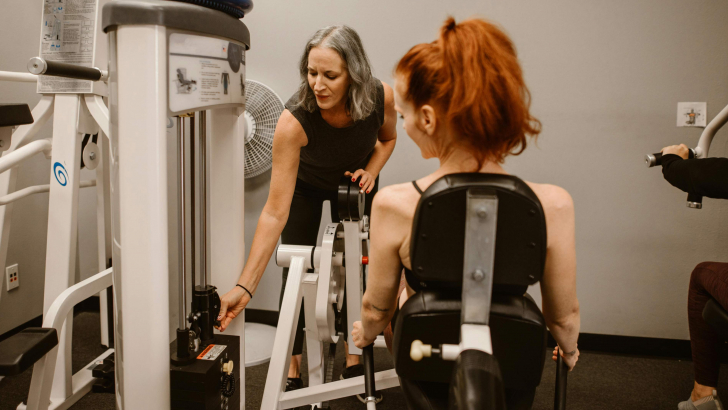MONDO SALUTE
In Salute. Test rapidi, vaccini e “infection control” contro l’antibiotico-resistenza
Non sono confortanti i dati riferiti poche settimane fa dall’Organizzazione per la cooperazione e lo sviluppo economico (Ocse) nel rapporto Embracing a One Health Framework to Fight Antimicrobial Resistance: il consumo di antimicrobici, sia nell'uomo che negli animali, rimane a livelli elevati. Nonostante gli sforzi politici per ottimizzare in particolare il consumo di antibiotici, si legge nel documento, le vendite medie di tutte le classi di antibiotici sono aumentate di quasi il 2% dal 2000, mentre più di un terzo dei Paesi Ocse non raggiunge l'obiettivo fissato dall'Organizzazione Mondiale della Sanità che prevede che gli antibiotici di prima linea (con uno spettro di attività ristretto) costituiscano almeno il 60% di tutto il consumo. Se le tendenze storiche continuano in questo modo, l'impiego di antibiotici nell'uomo non diminuirà in modo significativo almeno fino al 2035, con le conseguenze che ne derivano.
Oggi una infezione batterica su cinque nei Paesi Ocse non risponde al trattamento antibiotico, e ciò provoca la morte di circa 79.000 persone ogni anno: 2,4 volte il numero di decessi dovuti a tubercolosi, influenza e Hiv/Aids messi insieme nel 2020. Non mancano le ripercussioni anche sul piano economico: trattare le complicanze dovute a infezioni resistenti ha un costo che può superare i 28,9 miliardi di dollari all’anno, tenendo conto della parità di potere d’acquisto in 34 paesi Ocse e Ue/See. A fronte di questa situazione, il rapporto dell’Organizzazione per la cooperazione e lo sviluppo economico sottolinea l’importanza di aumentare gli investimenti nei pacchetti di azione One Health che mirano a contrastare la resistenza antimicrobica, con un ritorno sugli investimenti che sarebbe superiore ai costi di attuazione.
SULL'APPROCCIO ONE HEALTH LEGGI ANCHE:
Nel 2015 l'Organizzazione mondiale della Sanità ha lanciato il Global Action Plan on antimicrobial resistance, con l'obiettivo di mitigare l'emergere e la trasmissione di infezioni resistenti. Negli ultimi sei anni tuttavia sono stati compiuti pochi progressi nell'attuazione di programmi di prevenzione e di controllo delle infezioni e nell'ottimizzazione dell'uso di antimicrobici nel settore umano.
Nel nostro continente, lo scorso giugno il Consiglio europeo, in accordo con la Commissione europea, ha emanato una nuova raccomandazione per il potenziamento delle azioni di contrasto alla resistenza antimicrobica in ottica One Health, indirizzata ai governi degli Stati membri dell’Unione europea. Nel documento si incoraggia un uso prudente degli antimicrobici, in particolare degli antibiotici sia negli uomini che negli animali, per ridurre il rischio che i microrganismi diventino resistenti al trattamento farmacologico. In Italia, è il Piano nazionale di contrasto all’antibiotico-resistenza (Pncar) 2022-2025 a fornire al Paese le indicazioni per affrontare l’emergenza.
Facciamo il punto con Ivan Gentile, direttore della scuola di specializzazione in Malattie infettive e tropicali dell'Università degli Studi di Napoli e membro di Enaspoc-European Network for Antibiotic Steward-ship at the Point of Care. Una rete multidisciplinare, quest’ultima, orientata all'implementazione di azioni che migliorino la gestione degli antibiotici nelle cure primarie.
Antibiotico-resistenza, qualche riflessione sulle cause
La resistenza antimicrobica è la capacità dei microbi (batteri, virus, funghi, parassiti) di resistere agli agenti antimicrobici ed è una delle maggiori minacce per la salute pubblica a livello globale, con conseguenze sociali, economiche e sanitarie di vasta portata per persone, animali e ambiente. L’antibiotico-resistenza ne è un sottogruppo e si riferisce in modo particolare ai batteri che diventano resistenti agli antibiotici (farmaci che agiscono contro i batteri): questi medicinali, spiega Gentile, oltre ad avere un effetto sul singolo, hanno anche un’azione sull’ecologia dei batteri nella società.
“In Italia si fa un uso di antibiotici particolarmente elevato rispetto alle necessità, e le ragioni sono molteplici. Vengono utilizzati con molta frequenza per le infezioni virali, tanto che in tutto il mondo c’è un picco nell’impiego di questi farmaci nella stagione influenzale”. Spiega il docente: “Notoriamente l'influenza così come Covid-19 sono patologie virali, e gli antibiotici in questi casi non danno alcun beneficio, possono piuttosto recare un danno alla persona in caso di eventuali eventi avversi a breve termine, e soprattutto un danno sociale perché spingono le resistenze. La motivazione principale a mio avviso è culturale: c'è una proporzione di casi di infezioni batteriche che si sovrappongono alle infezioni virali, e nel dubbio il medico prescrive l'antibiotico. Sono anche i pazienti stessi a richiederlo, quasi come fosse la terapia risolutiva”.
Intervista completa a Ivan Gentile, professore di malattie infettive all'università di Napoli "Federico II". Servizio di Monica Panetto, montaggio di Barbara Paknazar
Test rapidi PCR
Esistono linee guida per una prescrizione appropriata degli antibiotici. L’Organizzazione mondiale della Sanità per esempio ha elaborato un manuale semplice e pratico per il loro utilizzo, l’AWaRe Antibiotic Book che fornisce istruzioni per la scelta dell’antibiotico, la formulazione, la dose e la durata di somministrazione. L’Aifa ha tradotto in italiano il volume.
Secondo Ivan Gentile, ci sono anche interventi che possono essere attuati. Uno di questi è l’impiego di test rapidi della proteina C reattiva (PCR). Il test può essere eseguito in sede ambulatoriale o al letto dell’ammalato: il risultato è disponibile già al momento della visita e orienta dunque alla prescrizione più appropriata. La PCR è una proteina di “fase acuta” prodotta dal fegato e presente in concentrazioni elevate nel sangue in caso di infiammazione dell’organismo. “Quando il valore è molto basso è inverosimile avere un'infezione batterica per cui in maniera estremamente convincente il medico comunica al paziente che non è necessario somministrare un antibiotico”. E davanti al risultato del test, la persona ammalata accetta più serenamente la decisione del dottore.
“A fini diagnostici il medico possiede mezzi classici, dunque visita l'ammalato, ascolta la sua storia, cerca di capire l'entità della sintomatologia. In molti casi però rimane un margine di dubbio che induce molto frequentemente a ordinare l'antibiotico. I test rapidi in questo setting potrebbero ridurre addirittura del 75-80% la prescrizione di antibiotici inappropriati”. Sono disponibili in commercio da tanti anni e fanno parte ormai dell'armamentario diagnostico del medico, sebbene siano ancora poco utilizzati. “Dal mio punto di vista i test rapidi sono destinati a diventare il futuro della medicina”. Gentile spiega che esistono test di molti tipi: alcuni consentono di rilevare infezioni delle vie urinarie, altri l'influenza, altri ancora Covid-19, come abbiamo ben imparato negli ultimi anni. “Il test della proteina C reattiva per la sua semplicità è quello che screma maggiormente chi necessita di antibiotico da chi può farne a meno”.
Vaccinazione e infection control
Sono anche altre le vie attraverso le quali si può contrastare la resistenza agli antimicrobici. “La vaccinazione è un'arma potentissima”. L'infettivologo spiega che se si riuscisse a somministrare il vaccino contro l’influenza in maniera proattiva non al 60% della popolazione come avviene oggi in Italia, ma si arrivasse al 90-95%, raggiungendo dunque non solo gli anziani ma anche chi lavora nelle scuole, nei centri commerciali, nelle officine, si ridurrebbe sicuramente anche il consumo di antibiotici. Oggi i vaccini disponibili sono molti, tra questi per esempio il vaccino contro lo pneumococco, batterio che può causare meningite, polmonite, sepsi e rendere necessario il ricorso all’antibiotico.
Ancor più importante secondo il docente è l’infection control, che si attua attraverso una serie di buone prassi utili a ridurre le infezioni, specie all’interno degli ospedali. “La procedura principe, la più semplice ma anche la più efficace, è il lavaggio delle mani. In Italia ci sono centinaia di migliaia di infezioni nosocomiali ogni anno e nel mondo forse milioni, e queste sono un carico enorme per i sistemi sanitari e per i pazienti innanzitutto. Le infezioni nosocomiali sono spesso indicate come malpractice nelle cause contro gli ospedali: la struttura sanitaria in quel caso deve dimostrare di aver fatto tutto il possibile per prevenire l'infezione e in ambito ospedaliero i batteri sono spesso molto resistenti”.
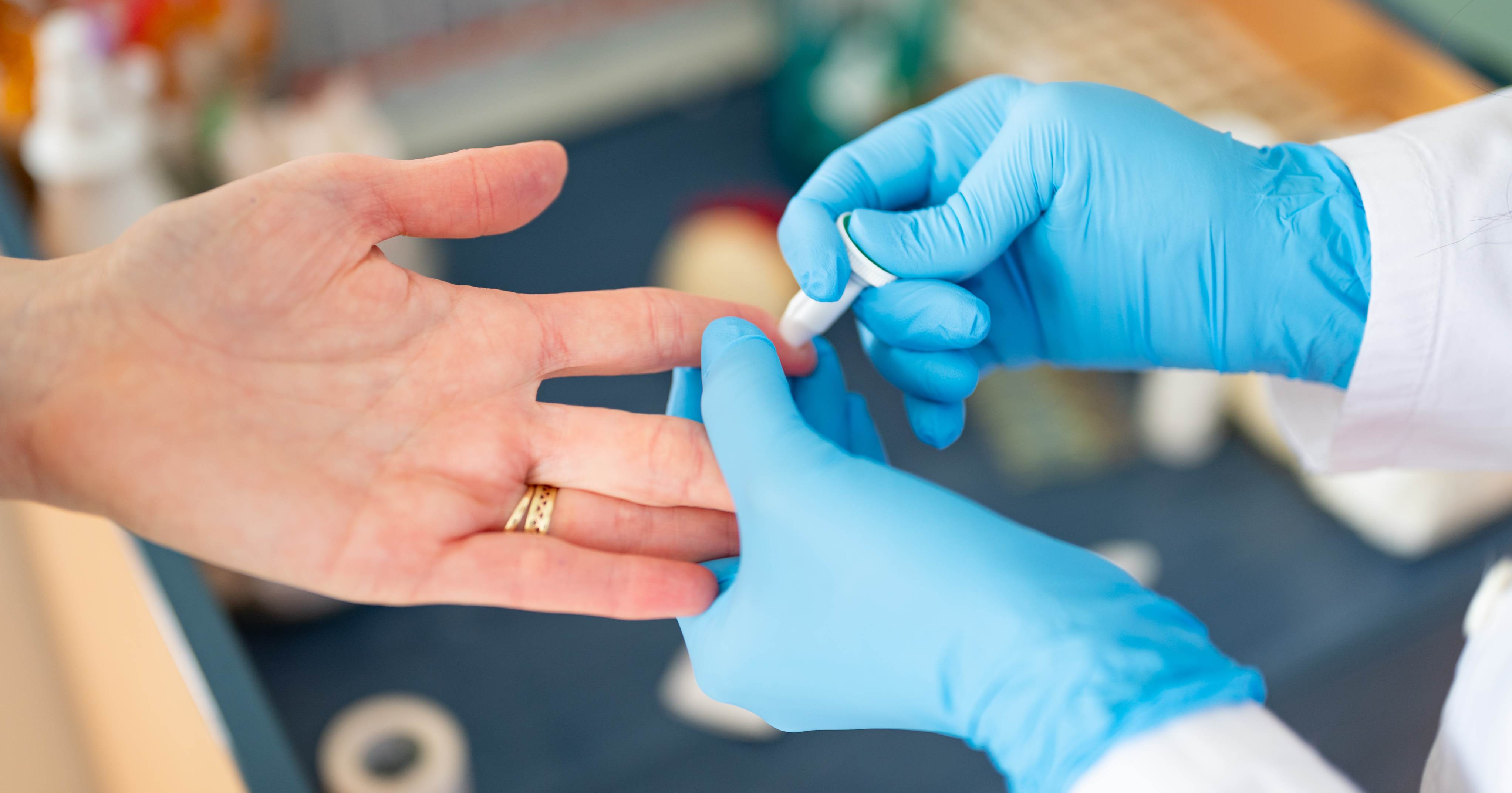
Il medico esegue il test PCR sulla paziente. Foto: Adobe Stock
Il Piano nazionale di contrasto all’antibiotico-resistenza e le azioni sul territorio
Il Piano nazionale di contrasto all’antibiotico-resistenza, come si è visto, fornisce al Paese indicazioni per contrastare il problema, seguendo un approccio One Health. I tre principali interventi di prevenzione e controllo dell’antibiotico-resistenza nel settore umano, animale e ambientale sono la sorveglianza e il monitoraggio integrato dell’antibiotico-resistenza, dell’utilizzo di antibiotici, delle infezioni correlate all’assistenza e il monitoraggio ambientale; la prevenzione delle infezioni correlate all’assistenza in ambito ospedaliero e comunitario e delle malattie infettive e zoonosi; l’uso appropriato degli antibiotici sia in ambito umano che veterinario.
“Attualmente – osserva Gentile – gli obiettivi raggiunti non sono molti, dal mio punto di vista dovremmo cambiare un po' il passo. Il Piano è estremamente ambizioso, ma oggi più che altro c’è la necessità che le Regioni verso le quali in Italia viene declinata l'attività ospedaliera, l’attività sanitaria in generale, possano avere la forza, gli strumenti e i finanziamenti per attuare il Piano, affinché non resti lettera morta”.
L’infettivologo spiega: “In Italia su 10 dosi di antibiotico 9 vengono assunte a livello territoriale e una in ospedale. Significa che il 90% circa degli antibiotici si consuma sul territorio. Quindi è lì che dobbiamo lavorare, dove si fa il maggior danno ecologico”. E uno degli interventi di più immediata attuazione, semplice ed economico da mettere in atto secondo Gentile, è l’impiego di test PCR rapidi a livello di cure primarie.
Il docente si sofferma anche sulla tipologia di medicinali somministrati: “Il nostro Paese utilizza globalmente meno antibiotici rispetto alla Francia, per esempio, ma più antibiotici ad ampio spettro (attivi su numerosi tipi di batteri, ndr). Questi però provocano maggiori danni ecologici rispetto a quelli con spettro di attività più ristretto. Dunque è importante imparare a utilizzare il primo tipo di farmaci solo quando è veramente necessario, così anche a parità di consumo si provoca un danno inferiore e si incide meno sulla resistenza”. La penicillina orale, per esempio, è un farmaco che in Italia praticamente non si usa più, diversamente da quanto accade nei Paesi nordici dove invece è ancora utilizzata. “Si tratta di un antibiotico a spettro molto limitato che si potrebbe ancora usare per molte indicazioni. In questo senso, si potrebbe ritagliare uno spazio sul territorio per vecchie molecole e lasciare che quelle a spettro più ampio vengano impiegate in ospedale, specie sui pazienti critici”. Questa linea, secondo Gentile, permetterebbe un utilizzo più appropriato degli antibiotici e, al tempo stesso, una razionalizzazione della spesa.