David Quammen: l’albero intricato e la resistenza antibiotica

Quando nel 2012 pubblicava Spillover, David Quammen riportava che The Next Big One, la prossima grande pandemia, “sarebbe stata causata da un virus zoonotico che viene da un animale selvatico, verosimilmente un pipistrello, probabilmente dopo essersi amplificato in un altro tipo di animale prima di passare agli esseri umani, poiché gli umani sono venuti forzatamente a contatto con questi animali, molto probabilmente in un wet market, magari situato in Cina, e che il nuovo virus si sarebbe rivelato particolarmente pericoloso se le persone contagiate gli avessero offerto un riparo, diffondendolo, prima di accusare alcun sintomo”.
Quando allo scrittore statunitense viene chiesto se sia un veggente o un profeta lui risponde: “Non sono stato preveggente, mi sono limitato a riportare in una forma composita ciò che alcuni esperti molto affidabili mi avevano preannunciato”.
Quest’anno è uscito per Adelphi “L’albero intricato” (The tangled tree, Simon & Schuster, 2018) e Quammen ne parlerà al Festival della Scienza di Genova in una Lectio magistralis sabato 24 ottobre.
L’albero cui il titolo fa riferimento è quello evolutivo, l’albero della vita. Sappiamo che la straordinaria diversità di forme viventi che oggi popolano il pianeta (e che la presenza umana sta seriamente mettendo a repentaglio) ha avuto origine da minuscole molecole che quasi 4 miliardi di anni fa hanno iniziato ad autoreplicarsi. Da Darwin in poi abbiamo capito che i rami dell’albero evolutivo crescono seguendo il principio di divergenza: gli organismi trasmettono verticalmente la propria eredità da una generazione all’altra e gli individui e le specie nel tempo si diversificano. Per lo meno questo è quello che vediamo a livello macroscopico. Ma quando andiamo a comparare gli organismi a livello molecolare scopriamo che la trama che descrive i loro rapporti di parentela è molto più intricata di quanto non potessimo immaginare. I nuovi metodi di analisi del Dna hanno permesso di scoprire che i rami dell’albero della vita dopo essersi separati talvolta possono tornare a riunirsi.
Il meccanismo che permette questa convergenza, che fino a pochi decenni fa si riteneva impossibile, è il trasferimento genico orizzontale “un movimento laterale di geni e segmenti di materiale genetico da una specie all’altra, persino da un regno della vita all’altro” spiega Quammen in questa intervista rilasciata a Il Bo Live. “A volte si parla proprio di eredità infettiva. I virus ad esempio sono in grado di prendere pezzi di Dna da un organismo che hanno infettato, riprodursi portando con sé quel segmento, e inserirlo nel Dna di un altro organismo che vanno a infettare. Questo è un esempio di trasmissione orizzontale di materiale genetico”.
Intervista a David Quammen, autore di "Spillover" e "L'albero intricato" (Adelphi). Montaggio di Barbara Paknazar
Carl Woese e la scoperta degli Archaea
David Quammen, con lo stile avvincente che lo contraddistingue, racconta la storia di molti scienziati e scienziate che hanno contribuito a costruire, mattoncino dopo mattoncino, questa nuova e per certi versi rivoluzionaria concezione dell’albero evolutivo. Una è la madre della teoria dell’endosimbiosi, Lynn Margulis. Grazie a lei oggi sappiamo che le cellule del nostro corpo sono figlie di una straordinaria e antica alleanza evolutiva tra un batterio (il mitocondrio) e una protocellula.
Ma il protagonista dell'intera vicenda è Carl Woese, microbiologo dell’università di Urbana-Champaign, Illinois: Quammen lo presenta come “il più importante biologo del ‘900 di cui non avete mai sentito parlare”. Grazie a nuovi metodi di filogenesi molecolare che lui stesso inventò e applicò, Woese rivoluzionò la nostra comprensione di come è organizzata la vita sulla Terra. Con l’aiuto di un suo post-doc, George Fox, analizzò una molecola presente in tutti gli organismi, l’Rna ribosomiale, e comparò le sequenze genetiche ottenute da organismi diversi. “Guardando a questa molecola puoi comparare batteri e cavalli, e vedere quanto sono diversi” spiega Quammen.
Nella seconda metà degli anni ‘70 analizzando una famiglia di microrganismi scoprì un nuovo raggruppamento che fino ad allora non era mai stato riconosciuto, “Per due-trecento anni si è pensato fossero batteri, ma non le erano. Queste cellule, nel modo in cui sono costruite, sono più simili a noi rispetto a quanto non lo siano ai batteri. Si iniziò a pensare che potessero essere le forme di vita complessa più antiche mai conosciute e per questo vennero chiamate Archaea”.
Fino agli anni ‘70 si pensava che gli organismi viventi si dividessero in procarioti (batteri, ovvero cellule semplici non dotate di strutture complesse come un nucleo) ed eucarioti (cellule complesse dotate di nucleo, come quelle del nostro corpo). Grazie Woese le radici dell’albero della vita sono diventate 3: batteri, Archaea ed eucarioti.
Ma la scienza vive di dibattiti, anche accesi, e di fatti James Lake, microbiologo dell’università della California, acerrimo rivale scientifico di Woese, la pensava diversamente. Secondo Lake i domini fondamentali dovevano essere 4. La disputa fu feroce e ancora oggi rimane accesa. Thijs Ettema dell'università di Uppsala in Svezia, ha scoperto nel 2015 un gruppo di microrganismi, i Lokiarchaeota, che ritiene possano essere simili a un antenato comune tra Archaea e eucarioti. “In questa visione ci sarebbero solo due rami fondamentali, batteri e Archaea, mentre il nostro non sarebbe nemmeno uno dei rami più importanti” spiega Quammen. “Tutti gli animali, le piante e i funghi (gli eucarioti) appartengono a una diramazione secondaria e discenderebbero da un antenato comune Archaea”.

Carl Woese, Jason Lindley/LAS, UIUC. Via Nature, 2018, John Archibald
Trasferimento orizzontale di geni
Tutti questi microrganismi (batteri, Archaea, virus) sono campioni di trasferimento orizzontale di geni, tanto che secondo Ford Dolittle, biologo statunitense membro della National Academy of Sciences, la trama della vita, a queste dimensioni, assomiglia più a una rete che a un albero.
A lungo molti scienziati hanno sostenuto che nonostante il trasferimento orizzontale di geni sia innegabile nei microgranismi, non sia altrettanto comune negli organismi complessi. “Molti lavori alla fine del secolo scorso hanno portato avanti l’eredità di Carl Woese e hanno mostrato che ci sono frammenti genetici che si spostano lateralmente anche negli organismi complessi, e lo hanno sempre fatto”. Esistono diversi meccanismi attraverso cui ciò avviene, uno di questi è proprio l’infezione virale. “L’8% del genoma umano è fatto di Dna virale che è stato portato nel ramo evolutivo dei mammiferi, dei primati e poi di noi umani nel corso di milioni di anni, da retrovirus. E lo hanno fatto anche nelle cellule del nostro sistema riproduttivo, rendendo quei pezzi di materiale genetico virale ereditabile da una generazione all’altra”. Alcune di queste introgressioni di Dna virale sono state molto utili per noi: insomma, esistono anche virus buoni. “Alcuni dei geni che contengono Dna virale sono essenziali per le funzioni biologiche umane, come la gravidanza: quello che una volta era il gene di un virus, una volta inserito nel genoma dei mammiferi è stato riadattato per costruire una membrana protettiva attorno al feto”.


"L'albero intricato", Adelphi, 2020; l'autore, David Quammen.
Resistenza antibiotica
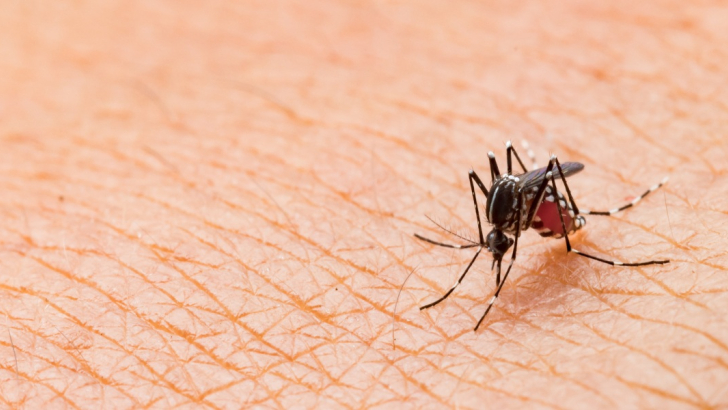
Il trasferimento orizzontale di geni è anche uno dei meccanismi fondamentali attraverso cui avviene la resistenza antibiotica, un fenomeno che Quammen definisce allarmante, al pari di quanto lo erano le zoonosi quando nel 2012 scriveva Spillover. “La resistenza antibiotica è un serio problema sanitario. Non so se diventerà mai tanto devastante nel breve termine quanto lo è la pandemia che stiamo vivendo. Ma so che è qualcosa a cui gli esperti stanno guardando con preoccupazione perché uccide già molta gente: decine di migliaia di persone solo negli Stati Uniti, centinaia di migliaia di persone nel mondo”.
Il rapporto sulla resistenza antibiotica diretto dall’economista Jim O’Neill e pubblicato nel 2016 ha stimato che nel mondo, nel 2050, le infezioni batteriche causeranno circa 10 milioni di morti all’anno, superando ampiamente i decessi per tumore (8,2 milioni), diabete (1,5 milioni) o incidenti stradali (1,2 milioni) con una previsione di costi che supera i 100 trilioni di dollari.
Sul sito dell’Aifa si legge che “In Europa si verificano annualmente 4 milioni di infezioni da germi antibiotico-resistenti che causano oltre 37.000 decessi e sono responsabili di un significativo assorbimento di risorse (sanitarie e non) che ammontano a circa 1,5 miliardi di euro l’anno; negli Stati Uniti sono 2 milioni i soggetti colpiti da un’infezione resistente agli antibiotici con circa 50 mila morti e una spesa che supera i 20 milioni di euro”.
I batteri possono diventare resistenti agli antibiotici in due modi. Uno è il classico processo di adattamento: se un’infezione batterica, ad esempio da stafilococco, viene trattata con antibiotici per lungo tempo, quel ceppo batterico può diventare resistente a quell’antibiotico. “Se io spargo l’insetticida nel mio campo magari uccido il 99% delle cavallette, ma l’1% che naturalmente sopravvive si riprodurrà e genererà individui che hanno questa propensione a sviluppare resistenza all’insetticida. È il processo di adattamento classico dell’evoluzione, ma è lento e graduale”.
Il secondo modo con cui i batteri possono sviluppare resistenza antibiotica è invece molto più veloce e fino a pochi anni fa sconosciuto. “Fu uno scienziato giapponese a scoprirlo, Watanabe. I batteri possono trasferire orizzontalmente i geni che li rendono resistenti agli antibiotici. Uno Staphilococcus aureus può impiegare anni a evolvere la resistenza a un antibiotico, ma una volta che l’ha evoluta può trasferirla, magari in una ferita infetta, a uno Streptococcus in un istante, ovvero a una specie di batterio completamente diversa”.
La resistenza antibiotica avviene soprattutto negli ospedali, spiega Quammen, dove convivono diversi tipi di infezioni e dove vengono utilizzati diversi tipi di antibiotici. “La pandemia da CoVid-19 e la resistenza antibiotica sono due fenomeni molto diversi, ma ciò che hanno in comune è che richiedono preparazione da parte nostra. Dobbiamo supportare la scienza, sia da un punto di vista finanziario sia intellettuale. Dobbiamo finirla con il negazionismo scientifico che è quasi una pandemia di per sé, specialmente nel mio Paese. Dobbiamo fidarci degli scienziati e degli esperti di politiche sanitarie. Dobbiamo far arrivare la scienza nelle scuole e dobbiamo formare nuove generazioni di scienziati a cui ci possiamo affidare”.