
L'Accademia delle Scienze di Stoccolma ha premiato Benjamin List e David W.C. MacMillan per “per lo sviluppo dell’organocatalisi asimmetrica”, che in sede di conferenza stampa è stato definito un "ingegnoso metodo per produrre molecole". Dal 2000, l'anno della scoperta indipendente dei gruppi capitanati dai due vincitori, questa scoperta si è rivelata di grande applicazione in diversi settori industriali, a cominciare dalla produzione di farmaci.
Una questione di velocità e tempo
Molto di ciò che ci circonda e utilizziamo ogni giorno è composto di molecole prodotte da una reazione chimica. A cominciare dall’ossigeno che respiriamo, fino alle plastiche compongono oggetti d’uso quotidiano e, appunto, i farmaci. A differenza di quando la reazione avviene in natura, nei processi industriali le reazioni sono spesso facilitate da catalizzatori. Sono a loro volta molecole che permettono alla reazione chimica di accelerare, accorciando enormemente il tempi di produzione delle molecole desiderate e rendendo così sostenibile la produzione.
Fino al 2000, solo due famiglie di catalizzatori erano conosciute: i catalizzatori metallici e gli enzimi. Spesso i metalli sono ottimi catalizzatori: hanno la capacità di ospitare temporaneamente gli elettroni o, al contrario, di fornirli ad altre molecole durante il processo chimico. Questa caratteristica rende più facile rompere i legami chimici, aumentando la probabilità che se ne formino di nuovi, sperabilmente quelli desiderati. Il problema è che per funzionare bene devono quasi sempre lavorare in assenza di ossigeno. Da ciò dipende la necessità di isolare le reazioni chimiche in contenitori dedicati che rendono difficile utilizzarli in produzioni su larga scala. Più efficienti sono gli enzimi, proteine che svolgono il ruolo di catalizzatore nelle reazioni organiche. Per esempio, nel nostro corpo ospitiamo una grande varietà di enzimi che sono essenziali per le reazioni chimiche che ci consentono di sopravvivere.
Il ruolo degli aminoacidi nella catalisi
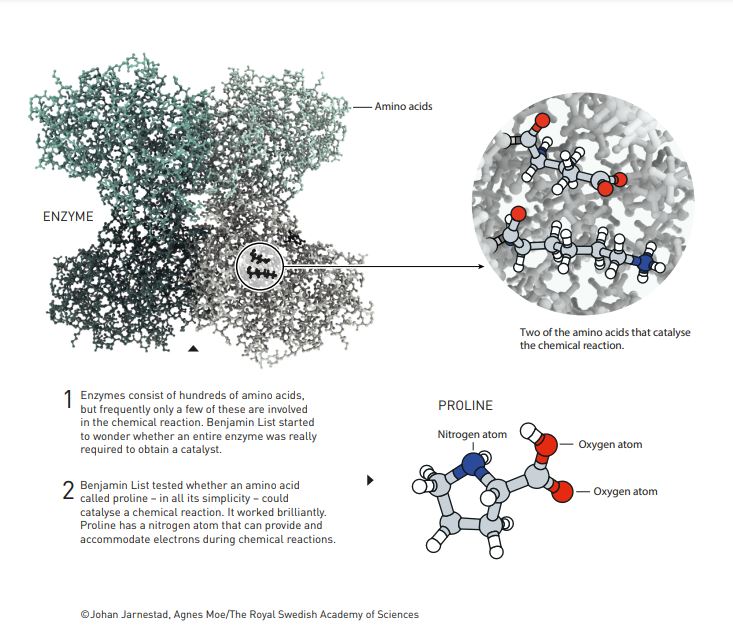
Benjamin List studiò a fondo l’effettivo funzionamento dei catalizzatori, in particolare gli enzimi. Si accorse che a guidare in modo particolare la loro attività erano particolari aminoacidi. Da questi primi esperimenti emerse l’idea di provare quindi a utilizzare gli aminoacidi come catalizzatori organici. In particolare cominciò a sperimentare la prolina, uno dei venti amminoacidi impiegati nella produzione delle proteine. È una molecola molto semplice, economica ed ecologica. Inoltre funziona meglio di catalizzatori metallici e degli enzimi: il sogno di ogni chimico industriale.
Dall’altra parte dell’oceano Atlantico, a Princeton (Stati Uniti) David MacMillan si accorse che molti dei catalizzatori che venivano prodotti dalla ricerca erano raramente impiegati nell’industria del tempo. A guidare la ricerca sua e del suo gruppo era provare a capire il perché e pensò che i catalizzatori metallici fossero semplicemente troppo difficili e costosi da usare. Raggiungere le condizioni di assenza di ossigeno e umidità richieste da alcuni catalizzatori metallici è relativamente semplice in un laboratorio, ma condurre una produzione industriale su larga scala in tali condizioni è complicato. Il sogno era quello di realizzare un catalizzatore che non dovesse per forza lavorare in ambiente privo di ossigeno e umidità.
Cominciò a pensare come poter progettare catalizzatori su base organica che avessero la stessa capacità di ospitare o fornire elettroni in fase di reazione. Selezionò diverse molecole organiche con le proprietà giuste e ne testò la capacità di guidare una reazione di Diels-Alder che i chimici usano per costruire anelli di atomi di carbonio. Proprio come aveva sperato e creduto, funzionò alla grande.
Una scoperta amica dell’ambiente
Il tipo di catalisi nata dalle scoperte di List e MacMillan è a base organica, ma viene anche definita asimmetrica. Che cosa significa? Quando avviene una reazione chimica in ambito industriale, il prodotto che ne risulta è spesso composto da una metà di molecole che è speculare all’altra metà, come se fossero una mano destra e una mano sinistra. Solitamente, però, solo una delle due tipologie è quello che vogliamo produrre.
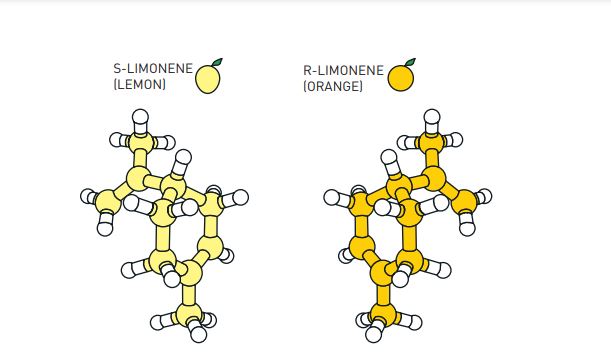
Una versione della molecola di limonene ha un profumo di limone, mentre la sua immagine speculare odora di arancia (Fonte: Nobel Prize Foundation)
Una delle motivazioni è che le due molecole speculari possono avere comportamenti diversi. Un caso storico eclatante è quello legato al talidomide negli anni Sessanta. Il talidomide era un farmaco sedativo e contro la nausea che è stato prescritto a molte donne in gravidanza. Una delle due tipologie di molecola provocava gravi deformità negli embrioni in via di sviluppo.
Le scoperte di List e MacMillan hanno dato origine a catalizzatori che oltre a velocizzare la reazione permettono di selezionare quale dei due tipi di molecole si vuole ottenere. In questo senso, si comportano in maniera asimmetrica. Questa loro caratteristica permette di evitare di mescolare le due versione speculari della stessa molecola, evitando potenzialmente danni come nel caso del talidomide. Ma significa anche ridurre notevolmente lo scarto, con un beneficio diretto anche sull’impiego delle risorse e dei materiali.




