Nobel alla Medicina: ecco le frontiere aperte dalle nuove scoperte
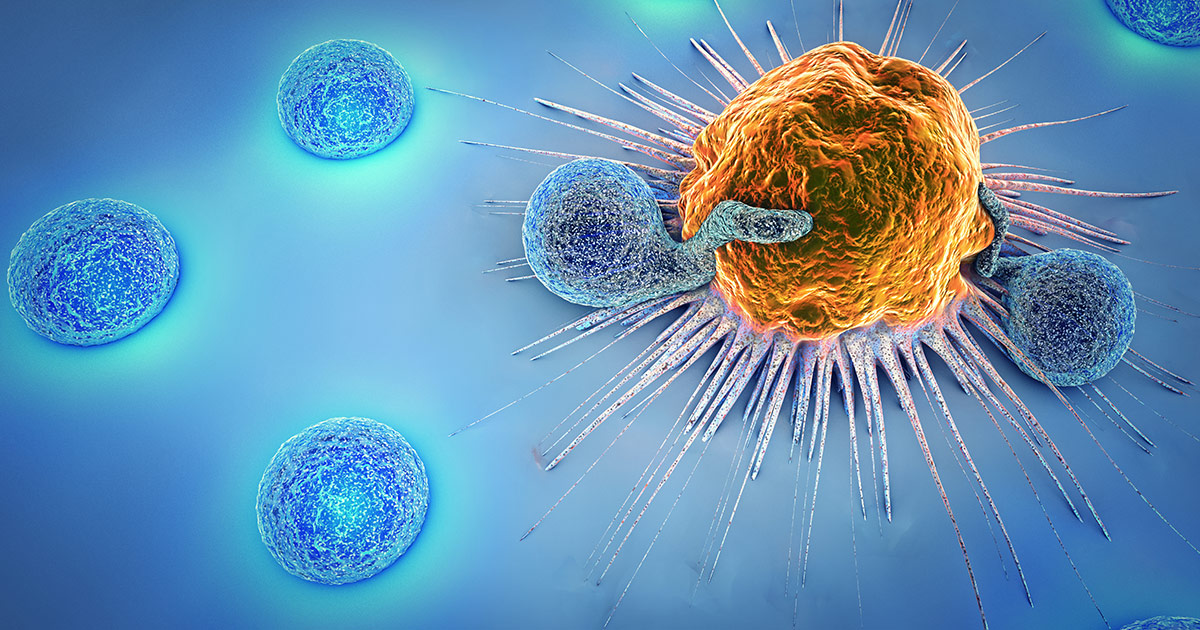
La notizia del conferimento del premio Nobel per la medicina 2018 agli Immunologi James Allison e Tasuku Honjo, per aver contribuito a stabilire un principio rivoluzionario per l’immunoterapia del cancro, è stata accolta con grande entusiasmo dalla comunità degli immunologi che lavorano in questo campo, ma anche con interesse e curiosità da un vasto pubblico di non addetti ai lavori. Curiosità in parte giustificata dalla spiegazione che spesso ha accompagnato la notizia: impiego degli inibitori dei checkpoint immunitari per “togliere il freno alle cellule del sistema immunitario e sguinzagliarle contro il tumore”.
Cosa significa in concreto questa spiegazione? In altre parole, cosa sono i checkpoint immunitari? Perché si usano gli Inibitori dei checkpoint immunitari come terapia del cancro? Quali nuove frontiere si sono aperte per l’immunoterapia nei tumori?
I checkpoint immunitari: quando devono funzionare e quando vengono utilizzati in modo improprio
Il sistema Immunitario ci difende dagli agenti patogeni utilizzando differenti popolazioni cellulari. Una di queste è rappresentata dai linfociti T, che sono capaci di svolgere un’azione specifica nei confronti delle cellule alterate a seguito dell’infezione, attaccandole e distruggendole. Il buon funzionamento del nostro sistema immunitario si basa su alcuni principi fondamentali. Uno di questi prevede che la risposte immunitaria si esaurisca quando l’agente patogeno è stato eliminato e l’azione distruttiva non è più necessaria. Il secondo principio stabilisce che la risposta immunitaria si attivi contro le cellule estranee o alterate, ma non nei confronti delle cellule sane del nostro corpo. Questo principio viene anche descritto come capacità del sistema immunitario di distinguere le cellule dell’organismo (“self”) dalle cellule estranee (“non-self”). Per rispettare queste condizioni, l’azione dei linfociti T è mantenuta costantemente sotto il controllo di sofisticati meccanismi conosciuti come checkpoint immunitari, che determinano quando un linfocita si debba attivare o meno.
I checkpoint immunitari sono proteine espresse sulla superficie dei linfociti T, chiamati anche recettori, capaci di inviare all’interno della cellula dei segnali che ne regolano la funzione. I segnali vengono innescati quando il linfocita prende contatto con una cellula presente nell’organismo, e deve decidere se attivarsi o meno. Il contatto viene stabilito dal legame dei recettori di checkpoint con altre proteine, chiamate ligandi, presenti sulla membrana della cellula con cui il linfocita si sta confrontando. In modo molto semplificato, possiamo immaginare che fra il linfocita T e la cellula con cui si confronta si svolga un dialogo, al termine del quale il linfocita capirà se la sua azione è opportuna o dannosa. In questo secondo caso, i controllori del processo ossia le proteine che fungono da checkpoint invieranno un segnale che frenerà l’azione del linfocita T.
Questa descrizione fa capire che difetti di funzionamento nei meccanismi di controllo possono comportare reazioni esagerate (nel caso una risposta immunitaria non si esaurisca), o reazioni improprie (nel caso che l’azione del linfocita T si eserciti verso una cellula sana dell’organismo, condizione che va sotto il nome di fenomeno autoimmunitario).
In questo scenario si inseriscono le ricerche degli scienziati premiati con il Nobel.
Le cellule tumorali possono essere riconosciute dal sistema immunitario dell’ospite. Infatti, nonostante siano cellule “self”, la trasformazione a cui vanno incontro durante il processo di sviluppo del tumore comporta la comparsa di molecole nuove, chiamate antigeni tumorali, che possono essere riconosciute dai linfociti T. La risposta immunitaria contro gli antigeni tumorali si può sviluppare se si realizzano tutte le condizioni necessarie per l’attivazione dei linfociti. È noto da tempo che il tumore mette in atto diverse strategie per evitare il riconoscimento e l’azione distruttiva del sistema immunitario; in certi casi diventa invisibile, in altri sopprime la risposta immunitaria. Una delle ultime strategie scoperta è proprio la possibilità che le cellule tumorali usino i checkpoint immunitari per evitare l’attacco del sistema immunitario, esprimendo in modo improprio i ligandi per i checkpoint e frenando così l’azione dei linfociti T, che riconoscendole come estranee le distruggerebbero.
Da queste conoscenze è partita la scommessa che ha portato al premio Nobel: utilizzare inibitori dei checkpoint per interrompere i segnali negativi inviati dalla cellula tumorale al linfocita T e consentire a quest’ultimo di esercitare la sua azione.
Gli inibitori dei checkpoint immunitari: cosa sono e come funzionano
Due sono le proteine di checkpoint che svolgono un ruolo chiave nei processi sopra descritti e su cui al momento si è concentrato lo sviluppo di nuovi trattamenti di immunoterapia. Si considera che esse agiscano in momenti diversi dello sviluppo di una risposta immunitaria.
La proteina CTLA-4, studiata da Allison, agisce nella fasi iniziali dell’attivazione di un linfocita T, tipicamente nei linfonodi dove la risposta immunitaria viene avviata.
La proteina PD-1, studiata da Honjo, interviene nelle cellule T già attivate, quindi nelle fasi più avanzate della risposta immunitaria, e tipicamente nei tessuti periferici dove l’azione dei linfociti si esplica.
Come già riportato, il nuovo concetto chiave dell’immunoterapia è che le cellule tumorali, avvantaggiandosi dell’espressione dei ligandi per queste proteine di checkpoint, di fatto si “camuffino” da cellule self, bloccando l’azione dei linfociti T. Pertanto, l’uso di inibitori dei checkpoint ha lo scopo di togliere questo freno e liberare l’azione dei linfociti T antitumorali.
Nuove frontiere per l'immunoterapia dei tumori
Gli strumenti che sono stati sviluppati come inibitori dei checkpoint sono anticorpi monoclonalidiretti contro le proteine sopra descritte.
Anticorpi monoclonali che bloccano CTLA-4 o PD-1 sono stati sviluppati e approvati per alcuni tumori, quali melanoma metastatico e cancro del polmone, che non rispondevano ad altri tipi di trattamento, ma il loro impiego si sta allargando anche ad altre neoplasie. Citiamo solo alcuni anticorpi monoclonali entrati nell’applicazione clinica. Contro CTLA-4 è già in commercio Ipilimumab (il suffisso “mab” sta per anticorpo monoclonale – Monoclonal Antibody), che nel melanoma metastaticoha dimostrato promettenti risultati. Il trattamento comunque non è scevro da effetti collaterali per il paziente. Contro PD-1è disponibile Nivolumab, in genere più tollerato, il cui impiego ha dato risultati anche superiori a Ipilimumab.
Per concludere, è importante ricordare che il ruolo fisiologico dei checkpoint è quello di prevenire la risposta dei linfociti contro le cellule self. L’impiego degli inibitori dei checkpoint toglie purtroppo il freno non solo ai linfociti T diretti contro il tumore ma più in generale mette in condizione anche tutti gli altri linfociti potenzialmente attivi contro il selfdi attaccare le cellule sane dell’organismo. Questo causa nei pazienti trattati una serie di effetti tossici collaterali in parte legati all’insorgenza di fenomeni autoimmunitari che si sviluppano in particolare in alcuni distretti, quali l’apparato gastroenterico, la cute, alcune ghiandole endocrine e altri organi.