Vaccino: incoraggianti i risultati di Oxford, in attesa di Cina e Stati Uniti
Shutterstock
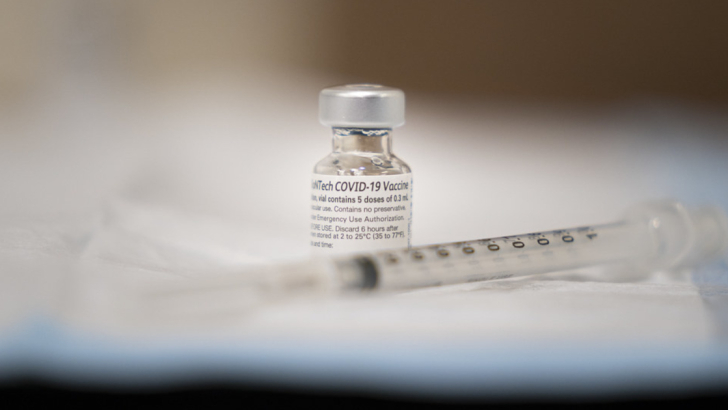
Le prime fasi di sperimentazione clinica del vaccino prodotto dall’università di Oxford hanno consegnato i primi risultati, pubblicati sulla rivista biomedica The Lancet, e sono incoraggianti. Non sono emersi effetti collaterali inaspettati e tutti i volontari cui è stato somministrato il vaccino hanno sviluppato una buona risposta immunitaria, sia per quanto riguarda il titolo anticorpale sia per quanto riguarda la produzione di linfociti T, un tipo di cellule capaci di immagazzinare una memoria immunitaria in grado di attivarsi di fronte a un nuovo attacco virale.
Circa 1000 volontari, residenti in Inghilterra, sono stati coinvolti nella sperimentazione: a 543 individui adulti compresi tra i 18 e i 55 anni è stato inoculato il vaccino sperimentale contro Sars-CoV-2 (ChAdOx1) sviluppato dal Jenner Institute dell’Università di Oxford in collaborazione con l’azienda anglo-svedese AstraZeneca; ad altri 534 è stato dato un vaccino di controllo, inefficace contro il nuovo coronavirus, per valutare le differenze di risposta tra il primo e il secondo gruppo (quello, appunto, di controllo).
I dati pubblicati su The Lancet dicono che tutti i pazienti che hanno ricevuto ChAdOx1 hanno sviluppato anticorpi entro i primi 28 giorni. A 10 volontari è stata somministrata anche una seconda dose del vaccino, che ha stimolato una risposta immunitaria ancora maggiore.
Dopo i risultati della sperimentazione in fase preclinica su un gruppo di macachi, anche il primo step della fase clinica mostra che lo sviluppo del vaccino oxoniense sta avanzando senza intoppi. “Siamo davvero contenti che il vaccino si stia comportando esattamente come pensavamo avrebbe fatto” ha commentato a The Guardian Sarah Gilbert, direttrice dello studio del Jenner Institute. “Abbiamo una certa dose di esperienza con questa tecnologia che abbiamo già usato in altri vaccini, quindi sapevamo cosa aspettarci, e abbiamo trovato esattamente quello che ci aspettavamo”.
Oxford’s Covid-19 vaccine produces a good immune response, reveals new study.
— University of Oxford (@UniofOxford) July 20, 2020
Teams at @VaccineTrials and @OxfordVacGroup have found there were no safety concerns, and the vaccine stimulated strong immune responses: https://t.co/krqRzXMh7B pic.twitter.com/Svd3MhCXWZ
La biotecnologia scelta dalla squadra di Oxford è quella del cosiddetto vettore virale: su un virus depotenziato che causa raffreddori negli scimpanzé (adenovirus) viene montato il gene di Sars-CoV-2 che esprime la proteina Spike e l’intero pacchetto viene iniettato nel corpo umano per stimolarne la risposta immunitaria. È una biotecnologia rodata e affidabile, la stessa che ha portato (a novembre 2019) al brevetto del vaccino che ha aiutato a vincere, a giugno di quest’anno, l’ondata di Ebola nel Congo orientale.
L’Italia e altri Paesi europei tra cui Germania, Francia e Paesi Bassi, avevano firmato già a giugno un accordo con AstraZeneca per la distribuzione di 400 milioni di dosi del vaccino, che risultava, allora come oggi, quello in stadio più avanzato di sviluppo. In Italia verrà anche prodotto il vaccino, dall’Irbm di Pomezia, mentre dell’infialamento si occuperà la Catalent di Anagni. Complessivamente AstraZeneca si è impegnata per produrre 2 miliardi di dosi vaccinali da distribuire in tutto il mondo.
Ad oggi sono 24 i vaccini contro Sars-CoV-2 che sono stati ammessi alla fase di sperimentazione clinica sull’uomo, 4 dei quali, stando al documento dell’Organizzazione mondiale della sanità aggiornato al 21 luglio, sono già entrati nella fase 3, quella in cui la sicurezza e l’efficacia sono già state valutate e in cui i trial clinici vengono estesi a decine di migliaia di persone di tutte le fasce d’età. Oltre che per quello di Oxford, la fase 3 è iniziata per 3 vaccini sperimentali sviluppati in Cina (Sinovac, Wuhan Institute e Beijing Institute in collaborazione con Sinopharm), tutti basati sulla biotecnologia del virus inattivato.
La CanSino Biologics non è ancora entrata nella fase 3 ma ha già fornito i risultati delle sue prime fasi di sperimentazione di un vaccino a vettore virale (adenovirus): un articolo su The Lancet uscito il 20 luglio riporta di circa 500 pazienti cui è stato inoculato il vaccino cinese e pressoché tutti risultano aver sviluppato una risposta immunitaria dopo 28 giorni, anche se alte dosi hanno prodotto seri effetti collaterali su 24 partecipanti. Il vaccino era già stato approvato dal governo cinese per una sperimentazione sui militari.
2 potential coronavirus vaccines from Oxford University and the Chinese company CanSino have triggered immune responses in hundreds of people without dangerous side effects, according to 2 studies published Mondayhttps://t.co/Do1Yl5anNF pic.twitter.com/4adSDh6NfJ
— The New York Times (@nytimes) July 20, 2020
Molto vicino alla fase 3 sarebbe anche il vaccino di Moderna, una della aziende statunitensi sostenute dai maxi finanziamenti del programma Warp Speed. Così come accaduto per il vaccino di Oxford, il 14 luglio sono stati pubblicati sul New England Journal of Medicine i risultati della fase 1 di sperimentazione del vaccino di Moderna, in collaborazione con gli scienziati del National Institute of Health (NIH): tutti i pazienti hanno sviluppato una risposta immunitaria soddisfacente in termini di quantità di anticorpi neutralizzanti, anche se i valori più alti sono stati raggiunti con una seconda iniezione a distanza di 4 settimane dalla prima. Più della metà dei volontari ha avvertito qualche lieve effetto collaterale come affaticamento, mialgia, mal di testa e dolore sul sito di iniezione. I risultati però sono relativi solo a 45 individui tra i 18 e i 55 anni e serviranno numeri molto più alti per valutare la reale efficacia di un vaccino, quello di Moderna, basato su una biotecnologia innovativa ma mai testata prima, il vaccino a Rna.
Anche la compagnia farmaceutica statunitense Pfeizer in collaborazione con la tedesca BioNtech ha riportato su MedRxiv il 20 luglio i risultati della sperimentazione di un vaccino a Rna su 60 persone. Nonostante il lavoro non sia ancora stato revisionato Pfeizer si è già accordata per la produzione di 100 milioni di dosi entro dicembre con il governo statunitense, che pagherà 1,95 miliardi di dollari.
Breaking News: Pfizer and a partner were given $1.95 billion to produce 100 million doses of a coronavirus vaccine by December. It needs to be vetted by the F.D.A. https://t.co/RPFS0Pknmb
— The New York Times (@nytimes) July 22, 2020
Ma serviranno ulteriori conferme anche dal vaccino di Oxford. La risposta immunitaria dei 1000 pazienti che hanno partecipato alla prima fase verrà monitorata per 12 mesi e nel frattempo una sperimentazione più grande è già in corso: nella fase 3 sono state reclutate decine di migliaia di individui (compresi minorenni e settantenni) non solo in Inghilterra, ma anche in Brasile, Sud Africa e negli Stati Uniti, dove il virus è ancora molto diffuso.
Sarà una strada lunga e non priva di ostacoli. Uno di quelli più ingombranti sembra essere la breve durata del titolo anticorpale dopo l’infezione: secondo uno studio del King’s College di Londra pubblicato su MedRxiv l’11 luglio, dopo circa due mesi dall’infezione solo il 17% di 65 pazienti aveva mantenuto un livello alto di anticorpi neutralizzanti. Secondo Rebecca Ashfield, Senior Project Manager dello Jenner Institue, questo potrebbe voler dire che anche laddove si ottenesse un vaccino efficace potrebbe essere necessaria una somministrazione annuale, come avviene per il virus dell’influenza stagionale.
Lo studio del King's College tuttavia non prende in considerazione i linfociti T, le cellule che mantengono la memoria immunitaria più a lungo termine. Un recente studio di un gruppo francese ha mostrato che è possibile guarire da CoVid-19 avendo pochissimi anticorpi neutralizzanti ma una elevata risposta delle cellule T. Per diversi studiosi il solo declino degli anticorpi neutralizzanti dopo qualche settimana dal recupero dall'infezione non significa che un futuro vaccino non sarà in grado di fornire una protezione di lunga durata. Ci sono ancora buone ragioni, dunque, per essere ottimisti.