L’autorizzazione a Sinopharm e la diplomazia vaccinale della Cina
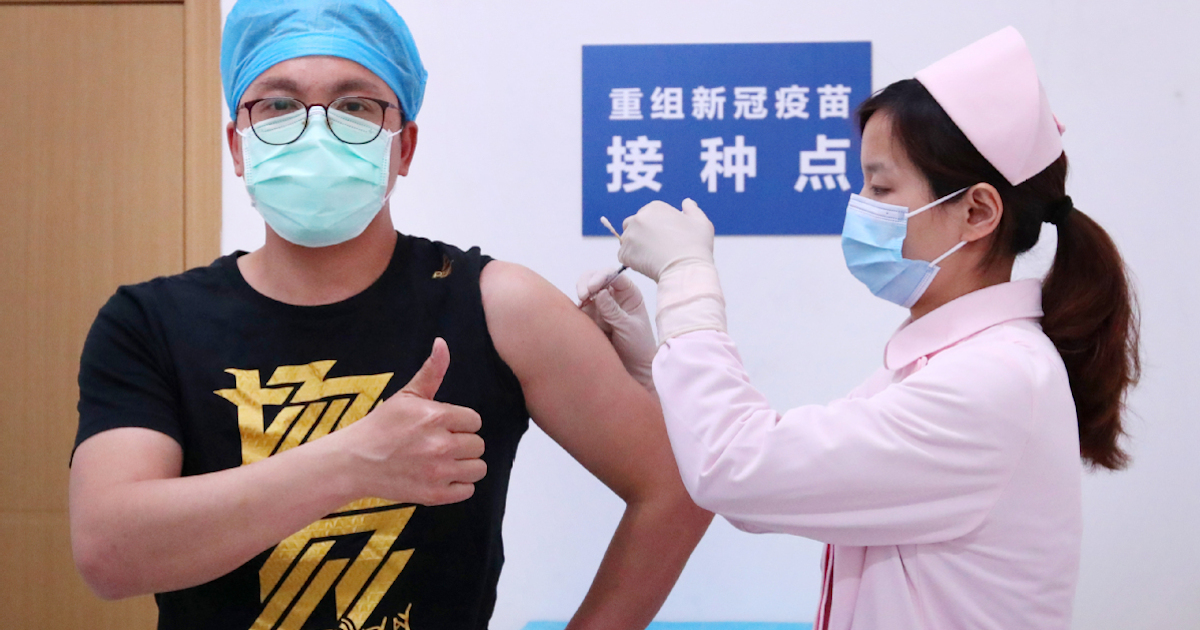
Foto di Zhu Xingxin, via China Daily
L’ultimo giorno del 2020 il governo cinese ha approvato l’uso del vaccino di casa sviluppato da Sinopharm (azienda farmaceutica controllata dallo Stato) in collaborazione con il Beijing Institute of Biological Products, dichiarandone un’efficacia del 79%. L’annuncio tuttavia non è stato accompagnato da un resoconto più dettagliato dei dati delle sperimentazioni.
Lo stesso vaccino era già stato approvato il 9 dicembre dagli Emirati Arabi Uniti e il 13 dicembre dal Barhain, Paesi in cui Sinopharm ha svolto alcuni dei suoi trial clinici. In quell’occasione entrambi avevano dichiarato un’efficacia dell’86%. Sinopharm però non aveva commentato l’annuncio.
La Cina dunque ora dispone di un altro vaccino da somministrare alla sua popolazione, dopo che a giugno aveva permesso la somministrazione di quello sviluppato da Cansino al corpo militare e agli operatori sanitari. L’obiettivo è quello di vaccinare 50 milioni di persone entro metà febbraio, periodo di svolgimento del capodanno cinese (12 febbraio 2021), un evento che prevede lo spostamento di quasi 600 milioni di persone, lo stesso che un anno fa è stato interrotto dalla comparsa di Sars-CoV-2.
Rispetto ai vaccini statunitensi di Pfizer e Moderna, basati sulla nuova tecnologia dell’RNA messaggero, che hanno un’efficacia di circa il 95%, e rispetto al russo Sputnik V, a vettore virale, con efficacia superiore al 90%, il vaccino di Sinopharm, basato sulla rodata tecnologia del virus inattivato, sembrerebbe avere un’efficacia leggermente minore, di poco inferiore all’80%. I suoi vantaggi risiedono però nel costo ridotto e nella facile trasportabilità.
L’approvazione del vaccino cinese era in qualche modo attesa, dopo le autorizzazioni rilasciate dai Paesi arabi. Tuttavia non deve stupire che sia arrivata qualche settimana dopo rispetto alle autorizzazioni rilasciate dagli Stati Uniti, dall’Europa e dal Regno Unito (che ha autorizzato quello di Astrazeneca, basato su adenovirus e con efficacia variabile dal 60% al 90% a seconda del dosaggio, nonostante gli ultimi studi concludessero che sarebbero state necessarie ulteriori analisi).
Le vaccinazioni in Cina infatti serviranno a mettere in sicurezza una popolazione che di fatto da diversi mesi è già tornata alla normalità. Hanno goduto di notevole diffusione mediatica ad esempio le immagini dei festeggiamenti per il nuovo anno a Wuhan.
Diversamente dagli e Usa e soprattutto dall’Europa, la Cina oggi non ha bisogno del vaccino per uscire dalla fase più critica della pandemia. Le misure draconiane messe in campo da Pechino già dalla prima ondata hanno abbassato la curva dei contagi e i rigidi sistemi di sorveglianza hanno mantenuto sotto controllo le nuove infezioni.
La bassa circolazione del virus in patria ha fatto sì che i trial clinici dei vaccini cinesi venissero effettuati all’estero, in Paesi come gli Emirati Arabi Uniti, Egitto, ma anche Turchia, Pakistan e Indonesia, snodi chiave della Belt and Road Initiative (BRI) nota anche come Nuova Via della Seta, un piano di investimenti e infrastrutture che lega gli interessi commerciali della Cina a una lista di oltre 100 Paesi. Ma i trial clinici dei vaccini cinesi sono stati svolti anche al di là dell’Oceano Atlantico, in Sud America – Brasile, Argentina, Cile (quest’ultimo partner della BRI) – e in Messico.
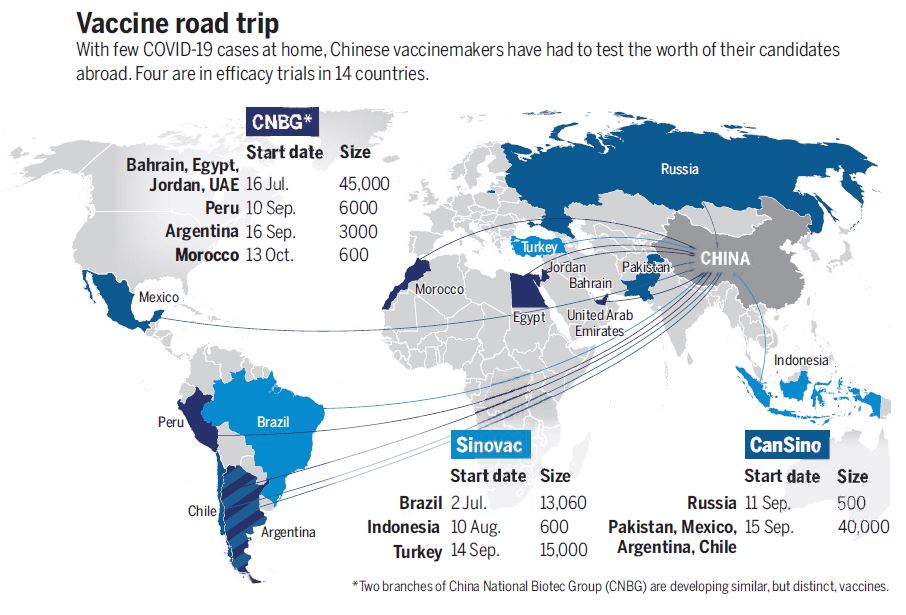
Mappa dei trial Paesi in cui i vaccini cinesi hanno svolo i trial clinici. Da "China's vaccine gambit", Science.
La scelta di stabilire un trial negli Emirati Arabi ha poi una valenza ulteriore. Il dinamismo di città come Abu Dhabi fa sì che qui vivano e lavorino persone provenienti da ogni parte del mondo. Ciò significa che i trial clinici svolti negli Emirati possono reclutare partecipanti provenienti da 125 Paesi diversi: dimostrare l’efficacia del vaccino qui significa mostrare la sua utilità per tutto il mondo.
Un vaccino cinese che si dimostri efficace e disponibile per molti Paesi, soprattutto quelli invia di sviluppo, dunque oltre a fornire una decisiva arma contro il virus svolgerebbe per la Cina almeno altre due funzioni extra-sanitarie: la prima sarebbe una notevole spinta all’immagine di Pechino nel mondo; la seconda sarebbe di natura diplomatica.
Intervistato da Science, Yanzhong Huang, esperto di salute globale della Seton Hall University (New Jersey) e membro del Council on Foreign Relations statunitense, sostiene che la Cina stia usando il vaccino per promuovere la diplomazia e raggiungere i suoi obiettivi in politica estera:
“La Cina vuole lavorare con questi Paesi e fornire loro la priorità per l’accesso al vaccino, perché ritengono che ciò possa facilitare l’implementazione della Belt and Road Initiative”.
Questa “diplomazia vaccinale” cinese è in netto contrasto con il “nazionalismo vaccinale” dell’operazione Warp Speed degli Stati Uniti.
Cina e Usa a confronto
A maggio il presidente Xi Jinping aveva annunciato all’Assemblea dell’Organizzazione mondiale della sanità (Oms) che quando il suo Paese avrebbe avuto un vaccino contro CoVid-19 lo avrebbe reso un bene pubblico globale. L’annuncio arrivava poco dopo la dichiarazione (di aprile) dell’allora presidente statunitense Donald Trump di tagliare i fondi all’Oms. L’uscita dall’organizzazione è stata ufficializzata a luglio, ma il neo presidente Joe Biden ha dichiarato di voler rientrare appena gli sarà possibile.
A ottobre Xi Jinping ha iscritto la Cina alla Covax Facility, l’iniziativa composta da Gavi, Cepi e Oms che mira a facilitare l’accesso ai vaccini da parte dei Paesi più poveri. A quest’alleanza invece non si sono uniti proprio gli Stati Uniti di Trump. L’operazione governativa Warp Speed poi ha investito diversi miliardi di dollari (inizialmente 10, poi saliti fino a 18) per accelerare lo sviluppo di vaccini statunitensi (come quello di Moderna), esteri (come quello di AstraZeneca) ma non cinesi, e per assicurarsi di ottenere il numero di dosi necessarie a vaccinare i 328 milioni di americani entro la fine del 2021.
Anche le retoriche adottate dalle due potenze in tema di vaccini si sono collocate agli antipodi. Bellicosa quella di Trump, che ha paragonato l’operazione Warp Speed al Progetto Manhattan. Sommessa quella di Pechino: la prima vaccinazione di un preparato sperimentale prodotto da Cansino avveniva già il 29 febbraio 2020, a poco più di due mesi dalla scoperta del virus. In quell’occasione furono vaccinati Chen Wei, medico ricercatrice e generale dell’esercito popolare cinese che aveva già lavorato al vaccino contro Ebola e che da gennaio si era messa al lavoro su Sars-CoV-2, e altri 6 scienziati militari.

Chen Wei, medico ricercatrice e generale dell'esercito popolare cinese, già nota per gli studi sul vaccino contro Ebola e da gennaio 2020 al lavoro sul vaccino contro Sars-CoV-2
La Cina non ha rivendicato primati globali, ma anzi è andata avanti per la sua strada e ha deciso di somministrare a una buona parte della popolazione vaccini che non avevano ancora iniziato trial clinici su larga scala. Cansino ha ricevuto l’autorizzazione all’uso emergenziale a giugno (pur senza dati pubblicati che ne provassero l’efficacia), ma anche gli altri tre principali vaccini cinesi (uno di Sinovac e altri due di Sinopharm) hanno ricevuto il semaforo verde per inoculare gran parte della popolazione al di fuori di trial clinici controllati e prima della loro dimostrata efficacia.
Funzionari del governo cinese in occasione dell’autorizzazione al vaccino di Sinopharm hanno dichiarato che 3 milioni di persone in Cina avrebbero già ricevuto le iniezioni protettive, con priorità a gruppi chiave della popolazione, come operatori sanitari, ma anche chi viaggia: il proprietario di un ristorante cinese di Padova infatti ha dichiarato di essersi fatto il vaccino in Cina a settembre. “La vaccinazione è completamente volontaria con consenso informato” ha fatto sapere CNBG (China National Biotech Group, società controllata da Sinopharm) a Science, e aggiunge: “non abbiamo ricevuto segnalazioni di un singolo caso di reazione avversa”. Secondo quanto riporta Science, a ottobre Sinovac avrebbe già messo in vendita a circa 60 dollari per due dosi il proprio vaccino in una città della provincia di Zhejiang, Yiwu.
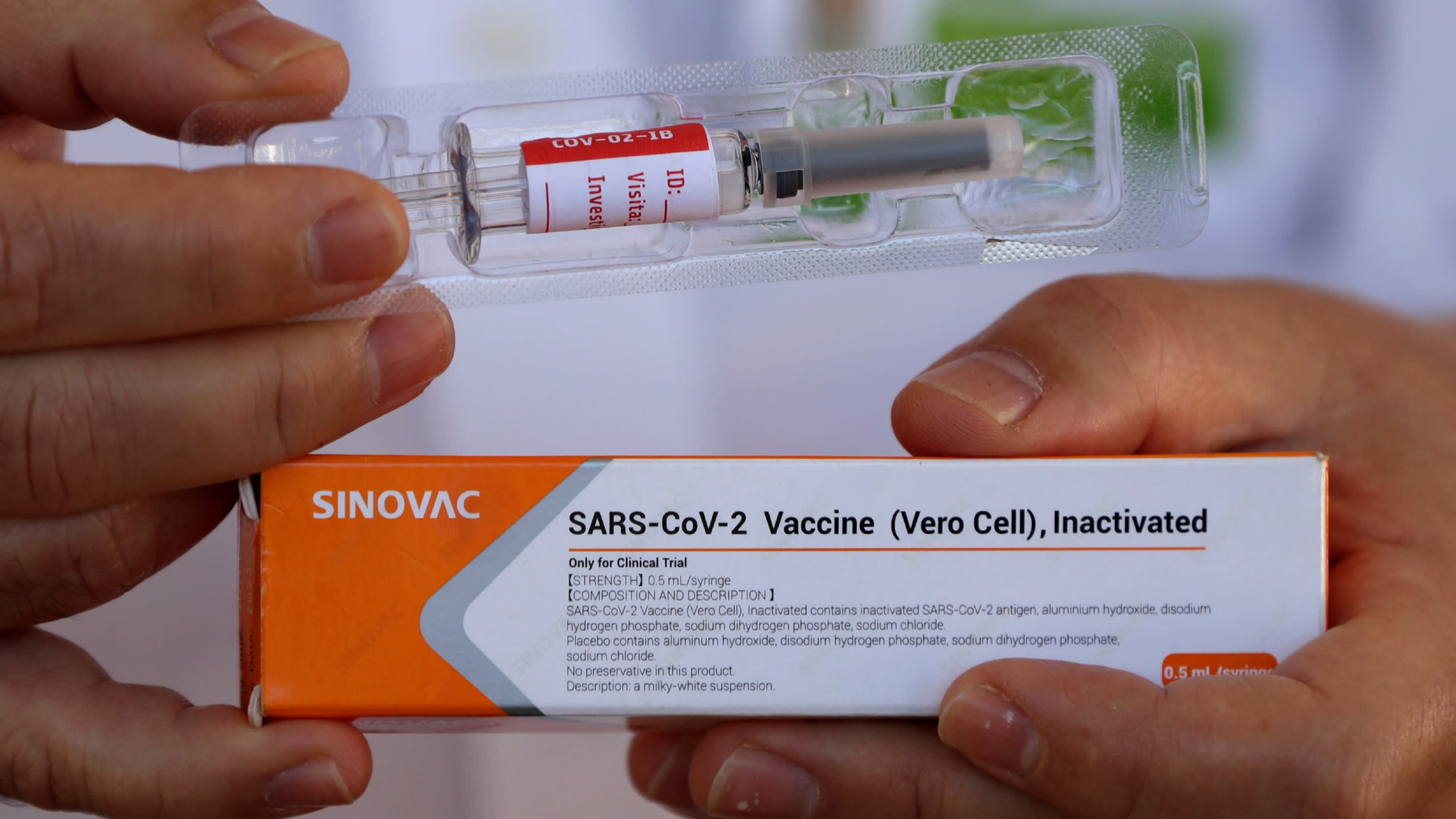
Vaccino Sinovac
Il mercato dei vaccini
A parte quello di Cansino, basato su adenovirus (la stessa tecnologia adottata da AstraZeneca e dal russo Sputnik V), gli altri tre vaccini cinesi in fase avanzata (uno Sinovac e due Sinopharm) sono basati sulla tecnologia del virus inattivato, lo stesso approccio che ha portato al primo vaccino anti-influenzale negli anni ‘30 del ‘900. Anche questa è una scelta radicalmente opposta rispetto a quella compiuta dalle statunitensi Pfizer e Moderna, che hanno puntato sull’innovativo mRna.
I cinesi hanno invece scelto, in un certo senso, l’usato sicuro, che non dovrebbe presentare sorprese e che dovrebbe garantire una buona efficacia (anche se inferiore rispetto a quelli a mRna). È inoltre facile da trasportare in quanto necessita solo di refrigerazione ordinaria (al contrario del vaccino a mRna, specialmente quello di Pfizer-BioNTech) e può essere messo sul mercato a costi accessibili.
San Paolo, in Brasile, ad esempio ha ordinato a Sinovac 46 milioni di dosi a un prezzo di 90 milioni di dollari, un costo 10 volte inferiore rispetto a ciò che il governo statunitense paga per i vaccini a mRna di Pfizer-BioNTech e Moderna (100 milioni di dosi del vaccino Pfizer sono costate agli Usa 1,9 miliardi di dollari).
La Cina ha dunque la possibilità di mettere sul mercato vaccini a un prezzo accessibile ai Paesi meno ricchi e concorrenziale rispetto alla maggior parte di quelli già approvati.
Secondo Reuters Europa e Stati Uniti pagheranno poco meno di 20 dollari a dose il vaccino Pfizer-BioNTech. Una stima più recente dice invece che l’Europa pagherà 12 euro a dose il vaccino Pfizer-BioNTech, mentre quello di Moderna dovrebbe costare intorno ai 18 euro a dose.
Più economico, sotto i 2 euro a dose, sarebbe quello di AstraZeneca approvato oltre che in Regno Unito, in Argentina il 30 dicembre e in India il 1 gennaio. La sua efficacia varia dal 60% al 90% a seconda del dosaggio, secondo gli studi pubblicati. Nonostante l’amministratore delegato di AstraZeneca, Pascal Soriot, abbia recentemente dichiarato un’efficacia del 95% (e del 100% nell’evitare casi gravi) l’Agenzia europea dei medicinali (Ema), così come la Fda statunitense, ha ritenuto improbabile una sua approvazione in Europa nel mese di gennaio (anche se non è da escludere),
Sullo scacchiere globale dunque se da un lato i vaccini più costosi, innovativi e (per ora) più efficaci sono stati ad oggi autorizzati e acquistati dai Paesi più ricchi che possono permetterseli, dall’altro si sta delineando un mercato parallelo, più vasto e non necessariamente meno redditizio, per i Paesi meno ricchi. La Cina è interessata a entrare con decisione in questo mercato, offrendo il vaccino certamente come cura, ma anche come strumento di scambio diplomatico. Ma non è la sola: l’India, che oltre ad aver autorizzato quello di AstraZeneca, ha approvato, il 3 gennaio, l’uso emergenziale del vaccino sviluppato dall’indiana Bharat Biotech, anch’esso a virus inattivato e potenzialmente accessibile ai Paesi in via di sviluppo.