Modelli animali per studiare il Covid-19: i risultati raccolti dall'OMS
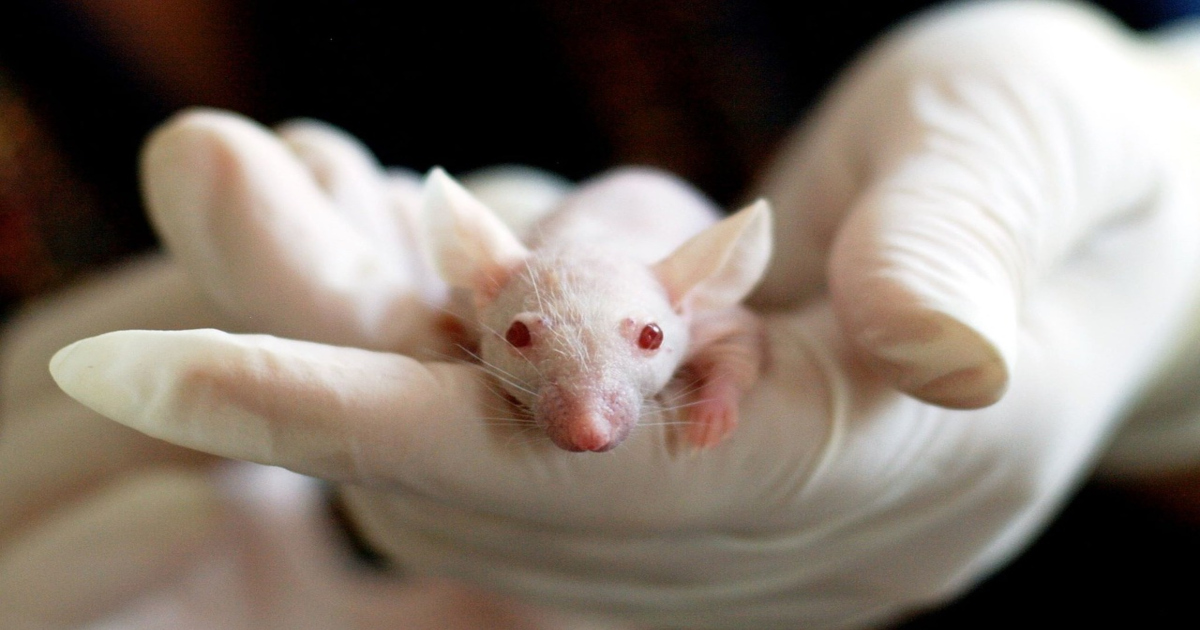
Fra le numerose caratteristiche del SARS-CoV-2 di cui è essenziale approfondire la conoscenza per poter sviluppare al più presto terapie e vaccinazioni efficaci vi è il meccanismo mediante il quale il virus infetta le cellule. Le numerose “punte” visibili nelle rappresentazioni microscopiche del coronavirus – quelle che gli conferiscono la sua peculiare forma “coronata” – sono le glicoproteine Spike (S), la cui funzione consiste nel legarsi alla cellula bersaglio aderendo al recettore ACE2 (Angiotensin-converting enzyme 2), un enzima presente nelle cellule di molti organi del nostro corpo, dai polmoni all’apparato gastro-intestinale (qui Francesco Suman, per Il Bo Live, spiega la genetica del coronavirus).
Come accade quando si studiano altre patologie, anche in questo caso un passaggio molto importante per la ricerca medica è la sperimentazione sugli animali. Poco dopo l’esplosione della pandemia, l’Organizzazione Mondiale di Sanità (OMS) ha istituito un gruppo di lavoro, nell’ambito del Progetto di Ricerca e Sviluppo (R&D Blueprint) attivato per far fronte all’emergenza, a cui è stato affidato il compito di raccogliere e monitorare tutti i modelli di studio (animali e non) sviluppati in relazione al SARS-CoV-2. I membri del gruppo di lavoro (OMS-COM: Covid-19 Modelling) hanno sottomesso, in giugno, i primi risultati delle ricerche, pubblicati da poco dalla rivista Nature.
Gli studi sono stati condotti principalmente su mammiferi, la classe animale che risulta più soggetta all’infezione: essi hanno, per ragioni evolutive, un sistema immunitario simile a quello umano. È importante, infatti, individuare quali siano gli animali più adatti ad essere utilizzati come modelli per studiare la patogenesi del virus negli esseri umani e per mettere a punto cure efficaci.
Topo domestico
I topi, gli animali da laboratorio per eccellenza, presentano, nel caso del coronavirus, un importante impedimento: nel Mus musculus – il topo domestico – mancano, infatti, i recettori ACE2 umani di cui, come accennato, il SARS-CoV-2 si serve per entrare nelle cellule ospiti e infettarle. Per ovviare a tale problema sono state messe a punto diverse strategie: alcuni ricercatori hanno provato a modificare la proteina Spike del SARS-CoV-2 in modo che si legasse al recettore ACE2 presente nei topi, mediante una progressiva selezione genetica del virus inoculato a più riprese nei tessuti polmonari degli individui. I topi resi suscettibili all’infezione hanno tuttavia presentato solo sintomi molto lievi.
Sono stati utilizzati, inoltre, tre diversi modelli di topi geneticamente modificati in cui è espresso il recettore ACE2 umano – creati in laboratorio ai tempi dell’epidemia di SARS, non a caso originata da un virus simile a quello attuale – che si sono tutti mostrati suscettibili all’infezione da SARS-CoV-2, con esiti patogenetici di diversa entità, da lievi a letali. Tali modelli, in cui sono stati rilevati sintomi come encefalite, trombosi, anosmia, possono essere utili per approfondire lo studio delle risposte immunitarie delle cellule T e per verificare possibili terapie farmacologiche e vaccinali. «Ad oggi – si legge nell’articolo – nessun modello tra quelli sviluppati con i topi ricapitola tutti gli aspetti del Covid-19 riscontrabili negli esseri umani, in particolare caratteri peculiari come le malattie vascolari polmonari e le sindromi iperinfiammatorie osservate, rispettivamente, in adulti e bambini».
Criceto dorato
Usati come modello anche per le infezioni causate da altri virus respiratori (come quello della SARS, quello dell’influenza e l’adenovirus), i criceti dorati o siriani (Mesocricetus auratus) sono risultati, da una comparazione computerizzata tra le sequenze del recettore ACE2 umano e di quello di questa specie, ampiamente suscettibili all’infezione da SARS-CoV-2. In seguito all’inoculazione del virus, i criceti hanno presentato sintomi anche gravi, tra cui difficoltà respiratoria, ma, tipicamente, la completa guarigione sopraggiungeva entro 14 giorni dal contagio. Interessante è il fatto che, nei criceti siriani, si sia rilevata una corrispondenza demografica con la decorrenza del virus nella popolazione umana: ad essere maggiormente colpiti erano, anche in questo caso, gli individui maschi e quelli in età più avanzata. Si sono potuti analizzare con successo, in questi animali, anche i meccanismi di trasmissione e la risposta immunitaria dell’organismo. Grazie alla versatilità e al basso costo di questo modello, lo si sta tenendo in considerazione anche per gli studi su possibili agenti terapeutici: dalle ricerche non emerge – riportano i ricercatori di R&D Blueprint – pressoché alcuna dimostrazione dell’efficacia di farmaci come l’idrossiclorochina e il favipiravir.
Furetto
Molto utili per comprendere la patogeneticità e le modalità di trasmissione del nuovo coronavirus sono anche gli esperimenti condotti sui furetti (Mustela putorius furo): le evidenze mostrano che «in questi animali, l’infezione sperimentale da SARS-CoV-2 comporta, in modo predominante, l’infezione del tratto respiratorio superiore. Ciò rende il furetto un valido modello per testare l’efficacia di vaccini mucosali e agenti terapeutici che mirano a prevenire l’infezione delle vie aeree superiori o la trasmissione mediante esse».

Macachi rhesus
Primati
Tra i primati, i test sono stati effettuati sui macachi (Macaca mulatta e Macaca fascicularis) e sulle scimmie verdi africane (Chlorocebus aethiops): risultati provenienti da diversi laboratori hanno mostrato alti livelli di replicazione virale per 7-14 giorni, con un interessamento sia del tratto superiore sia del tratto inferiore delle vie respiratorie, con sintomi sempre lievi e una risoluzione della malattia generalmente entro due settimane dal contagio. Diversi studi incentrati sulla somministrazione del vaccino hanno riportato un abbassamento della carica virale soprattutto nel tratto respiratorio inferiore: «Tali risultati evidenziano la possibilità che i vaccini siano più efficaci nel bloccare la malattia nel tratto respiratorio inferiore piuttosto che in quello superiore».
Gatto, cane, maiale
Studi condotti sui gatti hanno mostrato che questi animali sono fortemente soggetti all’infezione, e che possono facilmente contagiare loro simili sani, ma non vi sono evidenze della possibilità che trasmettano il contagio agli esseri umani. In ogni caso, il gatto non si è dimostrato un buon modello di studio – anche per le questioni etiche sollevate dall’impiego di animali domestici in esperimenti di laboratorio. Cani e maiali hanno mostrato, invece, una bassa risposta all’infezione, con eventuali sintomi presentatisi in forma molto lieve.
In generale, sembra che la diversità di risposte riscontrata in numerose specie di mammiferi sia dovuta non a mutazioni sopraggiunte nella struttura del SARS-CoV-2, quanto nei livelli di espressione del recettore ACE2 in questi animali, soprattutto nell’epitelio respiratorio. Altri studi, in cui si è riscontrata una discrepanza tra le predizioni dei modelli computerizzati e l’effettiva suscettibilità alle infezioni verificata nei laboratori, suggeriscono come la maggiore o minore possibilità di infezione dipenda da un diversificato insieme di fattori.
Le future ricerche – sottolineano gli autori – saranno utili soprattutto per stabilire la sicurezza e l’efficacia dei farmaci e dei vaccini che verranno sviluppati nei prossimi mesi: «I modelli animali sono necessari per valutare la possibilità che, in associazione al vaccino, vi siano patologie respiratorie più intense, e sarà importante istituire un efficace sistema di controllo per questa malattia».









